Đăng bởi : CÔNG TY TNHH THƯƠNG MẠI HÓA CHẤT VÀ THIẾT BỊ HOA VIỆT 16/08/2023
Axit Nitric là một trong những hợp chất hóa học có tính axit và oxy hóa mạnh được sử dụng rất rộng rãi trong đời sống hiện nay, nhất là với lĩnh vực sản xuất công nghiệp. Vậy hóa chất này có những tính chất đặc trưng gì, người ta điều chế chúng bằng cách nào và nó được ứng dụng cụ như thế nào trong các lĩnh vực? Hãy cùng HoaVietChem đi tìm hiểu về axit nitric qua nội dung bài viết dưới đây nhé!!!
I. Axit Nitric – HNO3 là gì?
Axit nitric có công thức hóa học là HNO3, được gọi là dung dịch nitrat hidro hay còn được gọi là axit nitric khan. Axit này được hình thành ở trong tự nhiên, tạo ra từ những cơn mưa do sấm và sét tạo thành.
II. Cấu tạo phân tử Axit Nitric – HNO3
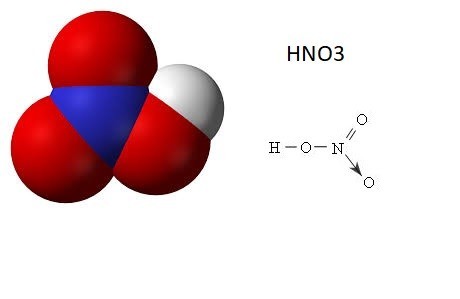
Cấu tạo phân tử - HNO3
III. Tính chất vật lý của axit nitric
- Axit nitric tồn tại ở dạng chất lỏng hoặc khí, không màu, tan nhanh trong nước (C, 65%). Hợp chất này trong tự nhiên sẽ có màu vàng nhạt do sự tích tụ của oxit nito.
- HNO3 là một axit có tính ăn mòn cao, dễ bắt lửa và cực độc.
- Axit nitric nồng độ 86% khi để ngoài không khí sẽ có hiện tượng khói trắng bốc lên.
- Tỷ trọng của axit nitric tinh khiết: 1511 kg/m3
- Nhiệt độ đông đặc: -41 độ C
- Nhiệt độ sôi: 83 độ C
- Dưới tác dụng của ánh sáng, axit nitric bị phân hủy tạo thành nito dioxit NO2 ( nhiệt độ thường).
4HNO3 → 4NO2 + 2H2O + O2
-
Cần bảo quản HNO3 trong các chai lọ tối màu, tránh nơi có ánh sáng và bảo quản ở nhiệt độ dưới 0 độ C.
- Axit nitric có thể hòa tan nito dioxit thành dung dịch có màu vàng hoặc đỏ ở nhiệt độ cao. Điều này ảnh hưởng không nhỏ đến các đặc trưng vật lý của chất này, đặc biệt là áp suất hơi trên chất lỏng, màu sắc dung dịch, nhiệt độ sôi,... phụ thuộc vào nồng độ NO2.
- Khi chưng cất hỗn hợp HNO3 và H2O ta thu thu được azeotrope có nồng độ 68% HNO3 và sôi ở 120,5 độ C, 1atm.

Axit nitric tồn tại ở dạng chất lỏng hoặc khí, không màu, tan nhanh trong nước
IV. Tính chất hóa học của HNO3
Axit nitric là một dung dịch nitrat hydro có công thức hóa học HNO3 . Đây là một axit khan, là một monoaxit mạnh, có tính oxy hóa mạnh có thể nitrat hóa nhiều hợp chất vô cơ, có hằng số cân bằng axit (pKa) = −2.
Axit nitric là một monoproton chỉ có một sự phân ly nên trong dung dịch, nó bị điện ly hoàn toàn thành các ion nitrat NO3− và một proton hydrat, hay còn gọi là ion hiđroni.
H3O+ HNO3 + H2O → H3O+ + NO3-
- Axit nitric có tính chất của một axit bình thường nên nó làm quỳ tím chuyển sang màu đỏ.
- Tác dụng với bazo, oxit bazo, muối cacbonat tạo thành các muối nitrat
2HNO3 + CuO → Cu(NO3)2 + H2O
2HNO3 + Mg(OH)2 → Mg(NO3)2 + 2H2O
2HNO3 + CaCO3 → Ca(NO3)2 + H2O + CO2
- Axit nitric tác dụng với kim loại: Tác dụng với hầu hết các kim loại trừ Au và Pt tạo thành muối nitrat và nước .
Kim loại + HNO3 đặc → muối nitrat + NO + H2O ( to)
Kim loại + HNO3 loãng → muối nitrat + NO + H2O
Kim loại + HNO3 loãng lạnh → muối nitrat + H2
Mg(rắn) + 2HNO3 loãng lạnh → Mg(NO3)2 + H2 (khí)
- Nhôm, sắt, crom thụ động với axit nitric đặc nguội do lớp oxit kim loại được tạo ra bảo vệ chúng không bị oxy hóa tiếp.
- Tác dụng với phi kim (các nguyên tố á kim, ngoại trừ silic và halogen) tạo thành nito dioxit nếu là axit nitric đặc và oxit nito với axit loãng và nước, oxit của phi kim.
C + 4HNO3 đặc → 4NO2 + 2H2O + CO2
P + 5HNO3 đặc → 5NO2 + H2O + H3PO4
3C + 4HNO3 loãng → 3CO2 + 4NO + 2H2O
- Tác dụng với oxit bazo, bazo, muối mà kim loại trong hợp chất này chưa lên hóa trị cao nhất:
FeO + 4HNO3 → Fe(NO3)3 + NO2 + 2H2O
FeCO3 + 4HNO3 → Fe(NO3)3 + NO2 + 2H2O + CO2
- Tác dụng với hợp chất:
3H2S + 2HNO3 (>5%) → 3Skết tủa + 2NO + 4H2O
PbS + 8HNO3 đặc → PbSO4 kết tủa + 8NO2 + 4H2O
Ag3PO4 tan trong HNO3, HgS không tác dụng với HNO3.
- Tác dụng với nhiều hợp chất hữu cơ: Axit nitric có khả năng phá hủy nhiều hợp chất hữu cơ, nên sẽ rất nguy hiểm nếu để axit này tiếp xúc với cơ thể người.
V. Điều chế axit nitric - HNO3
Trong tự nhiên, axit nitric được tạo ra từ các cơn mưa lớn có sét, gây nên những trận mưa axit.
1. Điều chế axit nitric - HNO3 trong phòng thí nghiệm
Người ta cho muối natri nitrat tinh thể tác dụng với axit sunfuric đặc, chưng cất hỗn hợp này tại nhiệt độ sôi của axit nitric là 83 °C cho đến khi còn lại chất kết tinh màu trắng. Tuy nhiên, phương pháp này chỉ tạo ra một lượng nhỏ axit.
H2SO4 đặc + NaNO3 (tinh thể) → HNO3 + NaHSO4
Axit nitric bốc khói đỏ thu được có thể chuyển thành axit nitric màu trắng. Khi thực hiện thí nghiệm , các dụng cụ phải làm từ thủy tinh, đặc biệt là bình cổ cong nguyên khối do axit nitric khan.
2. Điều chế axit nitric - HNO3 trong công nghiệp
Axit nitric loãng có thể cô đặc đến 68% axit với một hỗn hợp azeotropic với 32% nước. Để thu được axit có nồng độ cao hơn, tiến hành chưng cất với axit sunfuric H2SO4. H2SO4 đóng vai trò là chất khử sẽ hấp thụ lại nước.
4NH3 + 5O2 → 4NO + 6H2O (Pt, 850oC)
2NO + O2 → NO2
4NO2 + O2 + 2H2O → 4HNO3
Dung dịch axit nitric công nghiệp thường có nồng độ 52% và 68%. Việc sản xuất axit nitric được thực hiện bằng công nghệ Ostwald do Wilhelm Ostwald phát minh.
VI. Ứng dụng của axit nitric - HNO3 trong thực tiễn là gì?
Một số ứng dụng của axit nitric - HNO3
1. Trong phòng thí nghiệm
- Hợp chất axit nitric đa phần được sử dụng làm thuốc thử liên quan tới clorit. Người ta cho HNO3 tác dụng với mẫu thử, sau đó cho dung dịch bạc nitrat vào hỗn hợp để tìm kết tủa trắng của bạc clorua.
- Ngoài ra, axit nitric còn được sử dụng để điều chế muối nitrat.
2. Trong công nghiệp
- Axit nitric 68% được sử dụng để chế tạo thuốc nổ bao gồm trinitrotoluen (TNT), nitroglycerin, cyclotrimethylenetrinitramin (RDX), và các loại phân bón chứa ni-tơ như phân đạm một lá nitrat amoni NH4NO3, các muối nitrat như Ca(CO3)2, KNO3,...
- HNO3 nồng độ 0,5 - 2 % được dùng làm hợp chất nền nhằm xác định có kim loại tồn tại trong dung dịch hay không. Người ta gọi đó là kỹ thuật ICP-AES và ICP-MS. Để kết quả phân tích được chuẩn xác cần sử dụng HNO3 tinh khiết tuyệt đối.
- HNO3 phản ứng với hầu hết với các hợp chất hữu cơ nên nó được sử dụng nhiều trong ngành luyện kim, tinh lọc và xi mạ. Khi cho axit nitric tác dụng với axit clorua, ta được dung dịch cường toan có khả năng hòa tan và và bạch kim.
- Axit nitric còn được sử dụng trong sản xuất các chất hữu cơ, sơn, bột màu, thuốc nhuộm vải.
- HNO3 còn được dùng làm thuốc tẩy màu để phân biệt morphine và heroin.
- Hợp chất HNO3 được sử dụng để sản xuất nitrobenzen - tiền chất để sản xuất anilin và các dẫn xuất của nó - ứng dụng then chốt trong sản xuất sợi aramit, bọt xốp polyuretan và dược phẩm.
- Axit nitric còn là hợp chất trung gian trong sản xuất các chất kết dính, chất bộc phủ, chất bịt kín và các chất đàn hồi đi từ toluen diisoxyanat.
- Trong các nhà máy sữa, người ta dùng HNO3 làm chất tẩy rửa các đường ống, bề mặt kim loại.
- Axit nitric còn được sử dụng để loại bỏ các tạo chất và cân bằng lại độ tiêu chuẩn của nước.
- Một trong những ứng dụng khác cho IWFNA là một chất oxy hóa trong nhiên liệu lỏng tên lửa.






Bình luận (0)
Viết bình luận :